
Tuliskan Rumus Kimia Asam Basa Berikut.a Asam Klorida Bit CDN
Asam klorat adalah senyawa kimia yang terdiri dari unsur klorin, oksigen, dan hidrogen. Senyawa ini memiliki rumus kimia HClO3 dan biasanya ditemukan dalam bentuk kristal putih. Asam klorat digunakan dalam berbagai aplikasi, termasuk sebagai bahan bakar roket, pemutih kertas, dan penghilang gulma.
Rumus Kimia Asam Kromatofat Apa Itu Dan Bagaimana Cara Menghitungnya Riset
Berikut kami sajikan contoh asam kuat, asam lemah, basa kuat, basa lemah beserta rumus dan reaksi Ionisasinya. 7 Contoh asam kuat beserta rumus dan reaksi Ionisasinya. 1. Asam Klorida (HCl) Reaksi ionisasi: HCl → H+ + Cl- 2. Asam Nitrat (HNO3) Reaksi ionisasi : HNO3 → H+ + NO3- 3. Asam Sulfat (H2SO4) Reaksi ionisasi:

Rumus Kimia Larutan Asam Klorida Bit CDN
Pada senyawa asam, kata "asam" merupakan pengganti kata "hidrogen". Sehingga di awal kita tuliskan H. Ion klorat memiliki rumus kimia ClO 3-. Untuk mengetahui rumus kimia senyawa asam klorat, kita perlu mengecek muatan kation dan anionnya. Ion hidrogen memiliki muatan 1+ sehingga membentuk ion H +, sedangkan ClO 3- memiliki muatan 1-.

Reaksi Asam Basa Rumus Kimia Contoh Soal Dan Jawaban Riset
Ion klorat CAS # 14866-68-3 Struktur dan ikatan dalam ion klorat. Anion klorat mempunyai rumus ClO. Dalam kasus ini, atom klorin berada pada tingkat oksidasi +5. "Klorat" dapat juga merujuk pada senyawa kimia yang mengandung anion ini; klorat adalah garam dari asam klorat. "Klorat", jika diikuti dengan angka Romawi dalam kurung, misal klorat.
Rumus Kimia Senyawa Rumus Kimia 22196 Hot Sex Picture
Asam klorat adalah tergolong senyawa asam yang mengandung ion . Senyawa asam terdiri atas ion dan anion tertentu. Aturan penentuan rumus kimianya adalah: Langsung menggabung simbol ion dengan anoionnya serta menghilangkan muatannya jika muatannya sama. Menggabung simbol ion dan anion serta menyilangkan muatan menjadi indeks bagi dan anion, jika.

Rumus Kimia Molekul Asam Klorida Bit CDN
Baca Express tampilkan 1 Definisi Asam Klorat 2 Cara Membuat Asam Klorat 3 Manfaat Asam Klorat 4 Bahaya Asam Klorat 5 Kesimpulan 5.1 Sampai Jumpa Kembali di Artikel Menarik Lainnya! Hello Kaum Berotak, kali ini kita akan membahas tentang asam klorat yang memiliki rumus kimia yang cukup kompleks. Sebelum kita membahas lebih jauh tentang asam.
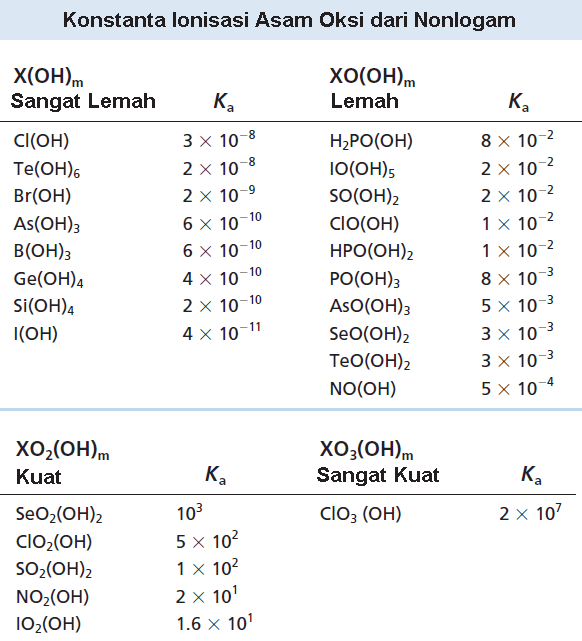
Rumus Kimia Asamasam Oksi dan Struktur Lewisnya Serba Ada
Kalium klorat adalah senyawa yang mengandung kalium, klorin dan oksigen, dengan rumus molekul KClO 3.Dalam bentuk murni, ia berupa kristal putih. Ini adalah klorat yang paling umum digunakan dalam industri. Garam ini digunakan sebagai oksidator,; untuk menghasilkan oksigen,; sebagai disinfektan,; pengaman korek api,; bahan peledak dan kembang api,; dalam budidaya, memaksa pemekaran pohon.

Rumus Kimia PDF
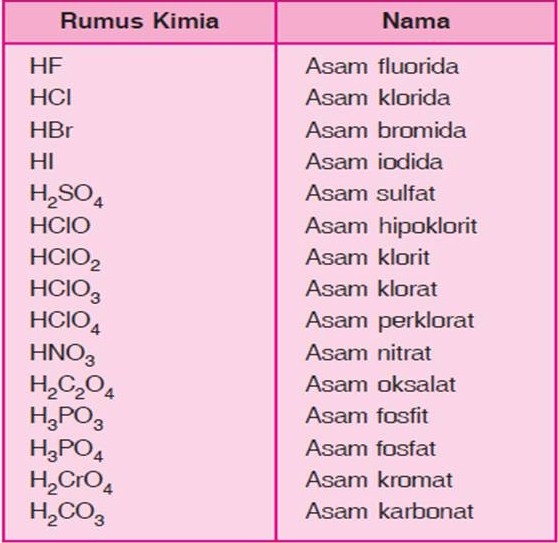
Daftar nama-nama asam beserta rumus kimia dan contoh kegunaannya dalam kehidupan sehari-hari.. Baca juga: Larutan Asam, Basa dan Garam. Asam Klorat (HClO3) Dilansir daru National Library of Medicine, asam klorat digunakan sebagai reagen dalam pembuatan berbagai macam senyawa kimia.

Tuliskan rumus kimia asam/basa berikut. a. Asam klorida b...
Komposisi Atom Senyawa Asam. Struktur molekul asam sulfat dengan rumus kimia H2SO4 yang memiliki komposisi 2 atom hidrogen (H), 1 atom sdulfut atau belerang (S) dan 4 atom oksigen (O). (chem.libretexts.org) KOMPAS.com - Senyawa asam memiliki rumus kimia yang biasanya diawali dengan H. Hal tersebut menandakan senyawa asam mengandung atom hidrogen.

Rumus asam dan basa
Berdasarkan penangkapan atau pelepasan oksigen. Oksidasi: reaksi yang melibatkan penangkapan atom oksigen. Contoh: C+ O2 → CO2. Atom C (karbon) mengalami oksidasi karena dalam reaksi atom karbon mengikat atom oksigen menjadi CO2. Reduksi: reaksi yang melibatkan pelepasan atom oksigen. Contoh: H2O2 → H2O + O2.

Rumus Kimia Asam Klorat Bit CDN
Asam iodida (HI) Asam klorat (HClO 4) Asam selain asam-asam di atas merupakan asam lemah, contoh: Asam askorbat; Asam karbonat; Asam sitrat; Asam etanoat; Asam laktat;. Rumus kimia asam sitrat adalah C 6 H 8 O 7. Sumber foto: Pixabay Sifat-sifat asam. Secara umum, asam memiliki sifat sebagai berikut:

Persamaan reaksi dari kalsium hidroksida + asam klorida menghasilkan kalsium klorida dan air
Asam klorit adalah suatu senyawa anorganik dengan rumus kimia HClO 2.Senyawa ini adalah asam lemah yang mengandung atom klorin dengan bilangan oksidasi +3. Zat murni senyawa ini bersifat tidak stabil, mudah mengalami disproporsionasi membentuk asam hipoklorit (bilangan oksidasi Cl adalah +1) dan asam klorat (bilangan oksidasi Cl adalah +5): . 2 HClO 2 → HClO + HClO 3

Sumber
Rumus kimia. HClO 3 Massa molar: 84.45914 g mol −1 Penampilan larutan bening Densitas: 1 g/mL, larutan (perkiraan) Kelarutan dalam air >40 g/100 ml (20 °C) Keasaman (pK a) ~ −1. Asam klorat, H Cl O 3, adalah suatu asam okso dari klorin, dan prekursor utama garam klorat.

Rumus Kimia Asam Klorat Bit CDN
Rumus, Kimia, Rumus Kimia, Ilmu Kimia, Materi Kimia SMA Kelas 10 11 12, Contoh Soal Kimia dan Penyelesaian, Materi Kimia Kurikulum 2013, Kimia K13. Rumus Kimia Asam Klorida - Terdapat rumus kimia asam klorida tersendiri yang nantinya RumusKimia.net akan bagikan kepada sahabat berikut ini.

Tuliskan Rumus Kimia Senyawa Magnesium Klorida Hot Sex Picture
Dalam larutan asam klorida, H+ ini bergabung dengan molekul air dan membentuk ion hidronium, H3O+: HCl + H2O → H3O+ + Cl-. Ion lain yang terbentuk ialah ion klorida, Cl-. Asam klorida oleh karenanya bisa digunakan untuk membuat garam klorida, seperti misalnya natrium klorida. Asam klorida ialah asam kuat karena asam klorida berdisosiasi penuh.

Rumus Kimia Asam Klorida Rumus Kimia
Asam perklorat adalah suatu asam mineral dengan rumus H Cl O 4.Senyawa ini biasa ditemukan sebagai suatu larutan tak berwarna, yang merupakan asam yang lebih kuat dari asam sulfat, asam nitrat dan asam klorida.Senyawa ini merupakan oksidator yang sangat kuat ketika panas, namun larutan berairnya hingga sekira 70% berat pada suhu kamar secara umum bersifat aman, dan hanya menunjukkan sifat.